Основные методы защиты металлов от коррозии
Основные методы защиты металлов от коррозии
Коррозия металлов и способы защиты от нее
| Коррозия – это процесс разрушения металлов и металлических конструкций под воздействием различных факторов окружающей среды – кислорода, влаги, вредных примесей в воздухе. |
Коррозионная стойкость металла зависит от его природы, характера среды и температуры.
- Благородные металлы не подвергаются коррозии из-за химической инертности.
- Металлы Al, Ti, Zn, Cr, Ni имеют плотные газонепроницаемые оксидные плёнки, которые препятствуют коррозии.
- Металлы с рыхлой оксидной плёнкой – Fe, Cu и другие – коррозионно неустойчивы. Особенно сильно ржавеет железо.
Различают химическую и электрохимическую коррозию.
| Химическая коррозия сопровождается химическими реакциями. Как правило, химическая коррозия металлов происходит при действии на металл сухих газов, её также называют газовой. |
При химической коррозии также возможны процессы:
Fe + 2HCl → FeCl2 + H2
2Fe + 3Cl2 → 2FeCl3
Как правило, такие процессы протекают в аппаратах химических производств.
| Электрохимическая коррозия – это процесс разрушения металла, который сопровождается электрохимическими процессами. Как правило, электрохимическая коррозия протекает в присутствии воды и кислорода, либо в растворах электролитов. |
В таких растворах на поверхности металла возникают процессы переноса электронов от металла к окислителю, которым является либо кислород, либо кислота, содержащаяся в растворе.
При этом электродами являются сам металл (например, железо) и содержащиеся в нем примеси (обычно менее активные металлы, например, олово).
В таком загрязнённом металле идёт перенос электронов от железа к олову, при этом железо (анод) растворяется, т.е. подвергается коррозии:
Fe –2e = Fe 2+
На поверхности олова (катод) идёт процесс восстановления водорода из воды или растворённого кислорода:
2H + + 2e → H2
O2 + 2H2O + 4e → 4OH –
| Например, при контакте железа с оловом в растворе соляной кислоты происходят процессы: |
Анод: Fe –2e → Fe 2+
Катод: 2H + + 2e → H2
Суммарная реакция: Fe + 2H + → H2 + Fe 2+
Если реакция проходит в атмосферных условиях в воде, в ней участвует кислород и происходят процессы:
Анод: Fe –2e → Fe 2+
Катод: O2 + 2H2O + 4e → 4OH –
Суммарная реакция:
Fe 2+ + 2OH – → Fe(OH)2
4Fe(OH)2 + O2+ 2H2O → 4Fe(OH)3
При этом образуется ржавчина.
Методы защиты от коррозии
Защитные покрытия
Защитные покрытия предотвращают контакт поверхности металла с окислителями.
- Катодное покрытие – покрытие менее активным металлом (защищает металл только неповреждённое покрытие).
- Покрытие краской, лаками, смазками.
- Создание на поверхности некоторых металлов прочной оксидной плёнки химическим путём (анодирование алюминия, кипячение железа в фосфорной кислоте).
Создание сплавов, стойких к коррозии
Физические свойства сплавов могут существенно отличаться от свойств чистых металлов. Добавление некоторых металлов может приводить к повышению коррозионной стойкости сплава. Например, нержавеющая сталь, новые сплавы с большой коррозионной устойчивостью.
Изменение состава среды
Коррозия замедляется при добавлении в среду, окружающую металлическую конструкцию, ингибиторов коррозии. Ингибиторы коррозии — это вещества, подавляющие процессы коррозии.
Электрохимические методы защиты
Протекторная защита: при присоединении к металлической конструкции пластинок из более активного металла – протектора. В результате идёт разрушение протектора, а металлическая конструкция при этом не разрушается.
Методы защиты от коррозии металлов

Методы защиты от коррозии металлов актуальны. Потому что металл является одним из самых востребованных материалов применяемых в автомобилестроении. И несмотря на то, что в некоторых областях его успешно заменяют, основная проблема, связанная с использованием металлических изделий это коррозия. Виды и методы защиты коррозии металла различаются друг от друга.
Коррозия, разрушение металла в результате электрохимического воздействия. Это растворение во влагосодержащей или воздушной среде электролита или химического воздействия, в результате которого происходит соединение металлов с химическими элементами, находящимися в воздушной или водной среде. Ржавление это коррозия железа и его сплавов, коррозия других металлов сводится к окислению, образованию оксидов. Химическая коррозия возникает в результате воздействия сухих газов и жидкостей, вступающих в химическую реакцию с металлом.
Виды коррозии металлов:
— процессы это химические и электрохимические
-по характеру разрушения равномерная, и не равномерная
— по виду коррозионной среды газовая, жидкостная, атмосферная, почвенная
Химическая коррозия
Основана на реакции между металлом и агрессивной средой. Результатом этой коррозии является образование на металле окалины или в случае с медью образуется зеленый налет. Этот тип коррозии распространяется равномерно по всей поверхности металла. Химическая коррозия не так сильно воздействует на металл, как электрохимическая.
Электрохимическая коррозия
Это процесс, при котором металлы и сплавы утрачивают часть своих электронов, они переходят в электролитический раствор, образующийся на поверхности металла в виде ионов, а электроны, замещающие атомы металла, переходят в металл с отрицательным зарядом, образуется гальваническая реакция в результате чего происходит разрушение металла. Металлы применяемые в строительстве подвергаются, как правило электрохимической коррозии, из за присутствия влаги на поверхности металла, вызвано это постоянным изменением температуры, в результате чего образуется конденсат.
Атмосферная коррозия
Атмосферная коррозия металла, аналогична протеканию электрохимической коррозии, в связи с наличием влажности воздуха. При повышении влажности свыше 70 процентов происходит интенсивная потеря стали. Также на процесс коррозии влияет наличие агрессивных элементов в окружающей среде таких как углекислый газ, диоксид серы,
По охвату поверхности коррозия может быть равномерная, при этом она не представляет большой опасности, если не достигает критических размеров повреждения металла. Наиболее опасна неравномерная коррозия металла Потому что могут образовывать отдельные очаги повреждения металла, что приведет к значительному ослаблению элементов металлической конструкции.
Избежать процессы коррозии, полностью невозможно, но снизить воздействие этих процессов возможно.
По видам различают несколько мер воздействия на коррозию.
Методы защиты от коррозии металлов
Методы защиты от коррозии металлов разделяются на технологические, активные и пассивные.
Активные методы
Методы защиты от коррозии металлов предполагают постоянное воздействие на металл, к ним относятся способы изменения коррозионной среды. Это снижение кислотности почвы, снижение содержания хлора в воде. Также к активному методу относится протекторная защита, она заключается в связывании металла с контактным материалом, который больше подвержен окислению, он называется протектором и по сути является громоотводом. Принимает на себя электролизные процессы, влияющие на ржавление металла.
Технологические приёмы
Это когда при производстве металла происходит добавление в стальной сплав хрома , титана, марганца, никеля, которые помогают получить сталь с антикоррозийными свойствами. Например при добавлении хрома на поверхности металла образуется оксидная пленка большой плотности
Пассивные методы
Происходит изолирование металла при помощи различных покрытий, которые препятствуют образованию коррозии. Применяют катодное и анодное покрытие.
Анодное покрытие
При применении анодного покрытия металл покрывают другим металлом с большим отрицательным потенциалом. Это как правило цинк, либо кадмий. В настоящее время распространена защита металла посредством нанесения слоя цинка.
Катодное покрытие
производится металлами с более положительным потенциалом. При катодном покрытии металла соблюдается механическая защита металла. В качестве катодного покрытия применяют олово медь. никель. Для покрытия металла применяют горячий метод, напыление, металлизацию, гальванизацию, При горячем методе сталь помещают в расплавленный металл, который покрывается тонким слоем. Горячий способ применяют при лужении, покрытие металла оловом, и цинкование.
Оксидирование
Также применят химические способы покрытия металла, это оксидирование, образуется оксидная пленка, которая защищает металл от коррозии, ещё этот процесс называют воронение стали. Также можно обработать сталь анодированием, это электролиз алюминия. Так же посредством фосфатирования и азотирования.
Применение эмалей и грунтов
Наиболее доступным методом защиты металла является применение специальных эмалей и грунтов.
Они осуществляют барьерную защиту от воздействия вредных факторов окружающей среды, она заключается в механической защите поверхности. Нарушение покрытия происходит при образовании микротрещин, в результате происходит возникновение подпленочной коррозии, для предотвращения проводят пассивацию поверхности металла, при помощи специальных лакокрасочных покрытий.
В состав, входят специальные химические агенты. К таким лакокрасочным покрытиям относятся грунты и эмали, имеющие в своём составе фосфорную кислоту, и другие ингибирующие элементы, замедляющие процесс коррозии. Более эффективными лакокрасочными материалами являются те которые осуществляют протекторную защиту. Это достигается путем добавления, в лакокрасочные покрытия металлов создающих донорские электронные пары, к ним относятся цинк, магний и алюминий.
Для защиты металлических конструкций, которые эксплуатируются в условиях промышленной атмосферы, разрабатываются специальные эмали, образующие, влагозащищающие уретановые покрытия. Для защиты от постоянного контакта с водной средой выпускаются эмали, способные наносится на цинк, медь и другие поверхности.
В настоящее время на рынке представлен широкий спектр антикоррозионных эмалей. Одним из новшеств является покрытие металла фторопластом, он обладает химической инертностью практически ко всем агрессивным средам. Эмали на его основе наносятся кистью, воздушным и безвоздушным распылением, на очищенную поверхность металла. При применении, того или иного материала необходимо учитывать факторы такие как вид металла условия его эксплуатации, производственные возможности и целесообразность использования.
Средства коррозионной обработки применяются в зависимости от марки металла, воздействующей среды, действующих на него нагрузок. Для каждой сферы эксплуатации конструкции предусмотрены нормативы. Оптимальным методом является, обработка металла в условиях завода. То есть нанесение, транспортировочного грунта.
Прежде чем он попадет на строительную площадку. Нанесение антикоррозионных материалов обеспечивают всего на всего 20 процентов защиты металла, основным фактором влияющим на качественную защиту металла является его предварительная обработка, от грязи . ржавчины, а также любых других веществ которые будут оказывать препятствие для окрашивания поверхности.
Обработка металла от коррозии
Механическая очистка поверхности при помощи щеток, скребков а также с применение электроинструмента с различными насадками
Пескоструйная очистка наиболее эффективный метод для очищения поверхности, но имеющий ряд недостатков, таких как низкая производительность, создание запыленности, что нарушает условия труда на строительной площадке.
Гидроструйная очистка повышает производительность, а применение абразивных материалов улучшает качество очистки.
Химическая очистка. Подразумевает применение специальных материалов которые разделяются на смываемые и несмываемые.
Смываемые методы химической очистки
К смываемым относятся 5% раствор соляной или серной кислоты, но при использовании этих материалов необходимо применять вещество, замедляющее химический процесс, так называемый ингибитор. Если не замедлить химическую реакцию помимо ржавчины уничтожится и сам металл. Можно использовать 15-30 % раствор ортофосфорной кислоты, в результате ее применения ржавчина превращается в твердую структуру, которая и является защитой от последующей коррозии. Хорошо помогает смесь 50 г молочной кислоты на 100 мл вазелинового масла. Кислота преобразует ржавчину в соль, а вазелиновое масло её растворяет.
Несмываемые методы химической очистки
Относят применение грунт преобразователей, ржавчина преобразуется в грунт, и не требует дальнейшего смывания. Если не удаётся полностью избавиться от ржавчины необходимо для предварительного окрашивания металла применить грунтовку со специальными антикоррозионными свойствами. Окончательная обработка поверхности производится с использование лаков, красок, эмалей со специальными свойствами.
Этапы антикоррозионных работ
- Подготовка необходимых материалов.
- Нанесение грунтовки обеспечивающей лучшее сцепление эмалей.
- Нанесение эмалей с защитным покрытием
- Сушка покрытия или его термообработка.
Наиболее эффективным способ нанесения лакокрасочных покрытии считается метод безвоздушного напыления. Так как он наиболее качественно позволяет прокрашивать. Имеющиеся неровности металла.
Менее эффективный способ это прокрашивание кистью. Нежелательно наносить лакокрасочные покрытия валиком.
Контроль качества выполненных работ
Применяемые методы защиты от коррозии металлов подвергаются контролю качества. Выполняется с целью проверки ранее выполненного производственного контроля. Предупреждение дефектов. Разработка мер по устранению обнаруженных дефектов. Контроль качества антикоррозионных работ начинается с проверки документации. Должны быть предоставлена документация на объект антикоррозионной защиты, на применяемые материалы, сертификаты о качестве продукции. По окончании проведения контроля качества работ составляется акт содержащий сведения о месте проведения работ, о состояния проведенных работ, о примененных материалах их марки и расходе. Сведения о организации исполнителе, и подписи лиц проводивших работы. Комиссия, проводящая контроль качества работ проверяет следующие параметры:
— вид антикоррозионного покрытия, не должно быть наличие мест не подвергнутых обработке.
— проверяется толщина слоя покрытия путем замера в различных местах, где предположительно возможна не качественная обработка.
— контролируется адгезия лакокрасочного материала с металлической поверхностью.
Нарушения выявляемые, при контроле качества работ.
После выполнения работ образуется ржавление на поверхности обработанного металла, это связано с тем что не был соблюден, температурный режим или не удалена полностью влага. Так же возможна недостаточная очистка металла от окислов, это приводит к возникновению последующей коррозии. Не достаточно убранные различные загрязнители масло, мыло, соли все это приведет к нарушению лакокрасочного покрытия дальнейшему ржавлению металла. Присутствие пыли на обрабатываемой поверхности снижает адгезию. Что приводит к отслоению лакокрасочного покрытия. Не выдерживание времени, которое допустимо на нахождение металла без обработки приводит к его ржавлению, также должна соблюдаться межслойная выдержка, растворитель не успевает раствориться и происходит его просачивание через другие слои. Что приводит к нарушению покрытия в виде пузырения. Все эти нарушения, выявленные при проведении контроля качества, подлежат немедленному устранению.
Методы защиты металлов от коррозии



Коррозионная стойкость — способность материала сопротивляться воздействию агрессивной среды. Она может определяться качественно и количественно: изменением массы образцов, показателей их физических и механических свойств, уменьшением толщины образцов, объема выделившегося водорода (или поглощенного кислорода) и др.
Коррозия причиняет огромные убытки. В результате нее металлические изделия теряют свои ценные технические свойства. Поэтому имеют очень большое значение меры борьбы с коррозией.
Они весьма разнообразны и включают следующие методы:
1. Защитные поверхностные покрытия металлов. Они бывают металлические и неметаллические. Металлические покрытия в свою очередь подразделяют на: гальванические; полученные, погружением в расплав; плакированием металлов; диффузионные и изотермически напыленные. Неметаллические покрытия бывают: силикатные (эмалированные); фосфатные; керамические, полимерные: лакокрасочные и порошкообразные.
3. Химический способ — применение ингибиторов коррозии.
4. Обескислороживание воды.
5. Создание сплавов с антикоррозионными свойствами.
Металлические гальванические покрытия изолируют металл от внешней среды. Их наносят электролитическим способом, подбирая состав электролита, плотность тока и температуру среды. Метод позволяет получать очень тонкие надежные слои металлов (цинк, никель, хром, свинец, олово, медь, кадмий и др.) и является экономичным. Покрытие железных изделий этими и другими металлами помимо защиты, придает им красивый внешний вид.
Тщательная очистка покрываемого изделия от загрязнений является одним из важных условий получения качественного покрытия. К загрязнениям относятся: жиры, масла и окислы. Обработку покрываемой поверхности производят тремя способами: механическим (шлифовка, песко- и дробеструйная очистка), химическим и электрохимическим (обезжиривание, травление и электрохимическое полирование). Хранение подготовленных изделий до покрытия не более 4 — 6 часов.
Например, кровельное железо предохраняют от коррозии цинком. Цинк, хотя и является более активным металлом, чем железо, покрыт снаружи защитной окисной пленкой. При ее повреждении возникает гальваническая пара железо-цинк. Катодом (положительным) служит железо, анодом (отрицательным) — цинк. Электроны переходят от цинка к железу, цинк растворяется, но железо остается защищенным до тех пор, пока слой цинка не разрушится до конца.
Методом погружения деталей в расплав наносятся например, покрытия из цинка и олова. Защитный слой (d = 10 — 50 мкм) имеет диффузионное сцепление с основой. Недостатки метода — трудность достижения равномерной толщины покрытия, а также большой расход металла, который например, при использовании цинка для слоя толщиной 25 мкм составляет до 600 г/м2.
Диффузионный способ защиты основан на изменении химического и фазового состава поверхностного слоя металла при вхождении в него подходящих элементов, которые обеспечивают коррозионную стойкость. Стали от атмосферной коррозии сохраняют цинкованием, алитирование применяют для защиты от окисления при повышенных температурах. Кремниевые покрытия (силицирование) используют для предохранения жаростойких металлов, борирование — для повышения износостойкости и прочности.
Плакирование металлов используют для изготовления биметаллических листов типа сталь-никель, сталь-титан, сталь-медь, сталь-алюминий. Его проводят методами совместного горячего пластического деформирования, электродуговой и электрошлаковой наплавкой, сваркой взрывом.
Напыляемые покрытия получают газотермическим, плазменным, детонационным и вакуумным способами. При этом металл распыляется в жидкой фазе в виде капель и осаждается на покрываемую поверхность. Метод прост, позволяет получать слои любой толщины с хорошим сцеплением с основным металлом. При вакуумном способе материал покрытия нагревают до состояния пара, и паровой поток конденсируется на поверхности изделия.
Методы напыления позволяют защищать сборные конструкции. Однако расход металла при этом очень значительный, а покрытие получается пористым и для обеспечения противокоррозионной защиты требуется дополнительное уплотнение термопластическими смолами или другими полимерными материалами. При восстановлении изношенных деталей машин пористость является весьма ценной, так как служит носителем смазочных материалов.
Стеклоэмалями называются стекла, наносимые тонким слоем на поверхность металлических предметов с целью защиты от коррозии, придания им определенной окраски и улучшения внешнего вида, создания отражающей поверхности и пр.
Производство эмалированных изделий включает в себя следующие операции: высокотемпературный синтез-варка эмалевых стекол (фриттов); приготовление из них порошков и суспензий; подготовка поверхности металлических изделий и собственное эмалирование — нанесение суспензии на поверхность металла, сушка и оплавление порошкообразного стекла в покрытие.
Стальные изделия грунтовой эмалью покрываются обычно двух- и трехкратно. Общая толщина получаемого покрытия в среднем равна 1,5 мм. После сушки полученного грунта при температуре 90 – 100 °С деталь далее обжигают при 850 – 950 °С. С целью увеличения долговечности эмалевых покрытий стальных труб в теплоэнергетике их наносят по слою напыленного алюминия.
В основе фосфатирования стальных изделий лежит процесс образования нерастворимых в воде двух- и трехзамещенных фосфатов железа, цинка и марганца. Они образуются при погружении изделий в разбавленный раствор фосфорной кислоты с добавкой однозамещенных фосфатов вышеперечисленных металлов. Получающийся фосфатный пласт хорошо сцеплен с металлической основой. Эти покрытия пористы, поэтому на них дополнительно нужно нанести лак или краску. Толщины фосфатных слоев составляют 10 – 20 мкм. Фосфатирование нужно вести окунанием или распылением.
В качестве керамической защиты используются покрытия на основе оксидов некоторых р-элементов, также кремниземистые, алюмисиликатные, магнезильные, карборундовые и другие. Получили развитие новые материалы, называемые керметы. Это металлокерамические смеси или комбинации металлов с керамикой, например Al — Al2O3 (САП), V – Al — Al2O3 (твэл). Они находят применение в реакторостроении. По сравнению с простой керамикой керметы обладают большей прочностью и пластичностью, имеют очень высокую сопротивляемость механическим и тепловым ударам.
Лакокрасочные покрытия наносят: распылением воздухом, высоким давлением и в электрическом поле; электроосаждением, струйным обливом, окунанием, валиками, кистью и т. д. Искусственная сушка красок может выполняться горячим воздухом, в камерах, инфракрасным и ультрафиолетовым излучениями.
Нанесение слоев из порошков полимеров осуществляют газопламенным, вихревым и электростатическим напылением. При температуре 650 –700 °С порошкообразный полимер размягчается и при ударе о подготовленную и нагретую до температуры давления полимера поверхность детали сцепляется с ней, образуя сплошное покрытие. Для напыления успешно используют полиэтилен, поливинилхлорид, фторопласты, нейлон и другие полимерные материалы.
Для катодной защиты стали в почве и нейтральных водных растворах минимальный потенциал составляет 770 – 780 мВ. Предусматривается одновременная пленочная изоляция поверхности изделия от контакта с коррозионной средой.
Анодную защиту применяют только для оборудования из сплавов, склонных к пассивации в данном технологическом растворе. Коррозия этих сплавов в инертном состоянии протекает гораздо медленнее. Используется источник постоянного тока с автоматическим регулятором потенциала анодной поляризации защищаемого металла.
В зависимости от агрессивности среды при анодно-протекторной защите применяют катоды из кремнистого чугуна, молибдена, сплавов титана и нержавеющих сталей. Так предохраняют теплообменники из нержавеющих сталей, работающие в 70 – 90 %-ной серной кислоте при температуре 100 –120 °С.
Ингибиторы коррозии — это вещества, замедляющие скорость разрушения металлических изделий. Даже в малом количестве они заметно снижают скорость обоих механизмов коррозии. Их вводят в рабочую агрессивную среду или наносят на детали. Они адсорбируются на металлической поверхности, взаимодействуют с ней с образованием защитных пленок и тем самым препятствуют протеканию разрушительных процессов. Некоторые антиоксиданты способствуют удалению кислорода (или другого окислителя) из рабочей зоны, что также снижает скорость коррозии.
Ингибиторами служат многие неорганические и органические соединения и разнообразные смеси на их основе. Их широко применяют при химической очистке паровых котлов от накипи, снятии окалины методом кислотной промывки, а также при хранении и перевозке неорганических сильных кислот в стальной таре и других. Например, для солянокислотной промывки теплосилового оборудования используют ингибиторы марок И-1-А, И-1-В, И-2-В (смесь высших пиридиновых оснований).
Создание сплавов с антикоррозионными свойствами заключается в легировании сталей такими металлами, как хром. При этом получают хромистые нержавеющие устойчивые к коррозии стали. Усиливают антикоррозионные свойства сталей добавками никеля, кобальта и меди. Легирование преследует достижение их высокой коррозионной стойкости в рабочей среде и обеспечение заданного комплекса физико-механических характеристик. Легирование сталей такими легкопассивирующимися металлами, как алюминий, хром, никель, титан, вольфрам и молибден придает первым склонность к пассивации при условии образования твердых растворов.
Для борьбы с МКК аустенитных сталей применяют:
а) снижение содержания углерода, что исключает образование хромистых карбидов;
б) введение в сталь более сильных, чем хром, металлов-карбидообразователей (титан и ниобий), что связывает углерод в их карбиды и исключает обеднение границ зерен по хрому;
в) закалку сталей от 1050 – 1100 °С, обеспечивающую перевод хрома и углерода в твердый раствор на их основе;
г) отжиг, обогащающий приграничные зоны зерен свободным хромом до уровня требуемой коррозионной стойкости.
Вопросы для самостоятельной работы. Основы теории коррозии, виды коррозии металлов, борьба и защита электрооборудования от коррозии Радиационные повреждения металлов и сплавов, борьба с радиационными повреждениями; исправление радиационных повреждений. Сварка и пайка в энергетике. Способы, сущность, преимущества и недостатки. Литература: Материаловедение. (Под общей ред. Б.Н. Арзамасова и Г.Г. Мухина) 3-е изд. переработанное и дополненное. М: Изд-во МГТУ им. Н.Э.Баумана, 2002.
Защита металла от коррозии
Металлы используются человеком с доисторических времен, изделия из них широко распространены в нашей жизни. Самым распространенным металлом является железо и его сплавы. К сожалению, они подвержены коррозии, или ржавлению — разрушению в результате окисления. Своевременная защита от коррозии позволяет продлить срок службы металлических изделий и конструкций.

Виды коррозии
Ученые давно борются с коррозией и выделили несколько основных ее типов:
- Атмосферная. Происходит окисление вследствие контакта с кислородом воздуха и содержащимися в нем водяными парами. Присутствие в воздухе загрязнений в виде химически активных веществ ускоряет ржавление.
- Жидкостная. Проходит в водной среде, соли, содержащиеся в воде, особенно морской, многократно ускоряют окисление.
- Почвенная. Этому виду подвержены изделия и конструкции, находящиеся в грунте. Химический состав грунта, грунтовые воды и токи утечки создают особую среду для развития химических процессов.
Исходя из того, в какой среде будет эксплуатироваться изделие, подбираются подходящие методы защиты от коррозии.
Характерные типы поражения ржавчиной
Различают следующие характерные виды поражения коррозией:
- Поверхность покрыта сплошным ржавым слоем или отдельными кусками.
- На детали возникли небольшие участки ржавчины, проникающей в толщину детали.
- В виде глубоких трещин.
- В сплаве окисляется один из компонентов.
- Глубинное проникновение по всему объему.
- Комбинированные.

Виды коррозионных разрушений
По причине возникновения разделяют также:
- Химическую. Химические реакции с активными веществами.
- Электрохимическую. При контакте с электролитическими растворами возникает электрический ток, под действием которого замещаются электроны металлов, и происходит разрушение кристаллической структуры с образованием ржавчины.
Коррозия металла и способы защиты от нее
Ученые и инженеры разработали множество способов защиты металлических конструкций от коррозии.
Защита от коррозии индустриальных и строительных конструкций, различных видов транспорта осуществляется промышленными способами.
Зачастую они достаточно сложные и дорогостоящие. Для защиты металлических изделий в условиях домовладений применяют бытовые методы, более доступные по цене и не связанные со сложными технологиями.
Промышленные
Промышленные методы защиты металлических изделий подразделяются на ряд направлений:
- Пассивация. При выплавке стали в ее состав добавляют легирующие присадки, такие, как Cr, Mo, Nb, Ni. Они способствуют образованию на поверхности детали прочной и химически стойкой пленки окислов, препятствующей доступу агрессивных газов и жидкостей к железу.
- Защитное металлическое покрытие. На поверхность изделия наносят тонкий слой другого металлического элемента — Zn , Al, Co и др. Этот слой защищает железо о т ржавления.
- Электрозащита. Рядом с защищаемой деталью размещают пластины из другого металлического элемента или сплава, так называемые аноды. Токи в электролите текут через эти пластины, а не через деталь. Так защищают подводные детали морского транспорта и буровых платформ.
- Ингибиторы. Специальные вещества, замедляющие или вовсе останавливающие химические реакции.
- Защитное лакокрасочное покрытие.
- Термообработка.

Порошковая покраска для защиты от коррозии
Способы защиты от коррозии, используемые в индустрии, весьма разнообразны. Выбор конкретного метода борьбы с коррозией зависит от условий эксплуатации защищаемой конструкции.
Бытовые
Бытовые методы защиты металлов от коррозии сводятся, как правило, к нанесению защитных лакокрасочных покрытий. Состав их может быть самый разнообразный, включая:
- силиконовые смолы;
- полимерные материалы;
- ингибиторы;
- мелкие металлические опилки.
Отдельной группой стоят преобразователи ржавчины — составы, которые наносят на уже затронутые коррозией конструкции. Они восстанавливают железо из окислов и предотвращают повторную коррозию. Преобразователи делятся на следующие виды:
- Грунты. Наносятся на зачищенную поверхность, обладают высокой адгезией. Содержат в своем составе ингибирующие вещества, позволяют экономить финишную краску.
- Стабилизаторы. Преобразуют оксиды железа в другие вещества.
- Преобразователи оксидов железа в соли.
- Масла и смолы, обволакивающие частички ржавчины и нейтрализующие ее.

При выборе грунта и краски лучше брать их от одного производителя. Так вы избежите проблем совместимости лакокрасочных материалов.
Защитные краски по металлу
По температурному режиму эксплуатации краски делятся на две большие группы:
- обычные, используемые при температурах до 80 °С;
- термостойкие.
По типу связующей основы краски бывают:
- алкидные;
- акриловые;
- эпоксидные.
Лакокрасочные покрытия по металлу имеют следующие достоинства:
- качественная защита поверхности от коррозии;
- легкость нанесения;
- быстрота высыхания;
- много разных цветов;
- долгий срок службы.
Большой популярностью пользуются молотковые эмали, не только защищающие метал, но и создающие эстетичный внешний вид. Для обработки металла распространена также краска-серебрянка. В ее состав добавлена алюминиевая пудра. Защита металла происходит за счет образования тонкой пленки окиси алюминия.

Эпоксидные смеси из двух компонентов отличаются исключительной прочностью покрытия и применяются для узлов, подверженных высоким нагрузкам.
Защита металла в бытовых условиях
Чтобы надежно защитить металлические изделия от коррозии, следует выполнить следующую последовательность действий:
- очистить поверхность от ржавчины и старой краски с помощью проволочной щетки или абразивной бумаги;
- обезжирить поверхность;
- сразу же нанести слой грунта;
- после высыхания грунта нанести два слоя основной краски.
При работе следует использовать средства индивидуальной защиты:
- перчатки;
- респиратор;
- очки или прозрачный щиток.
Способы защиты металлов от коррозии постоянно совершенствуются учеными и инженерами.
Методы противостояния коррозионным процессам
Основные методы, применяемые для противодействия коррозии, приведены ниже:
- повышение способности материалов противостоять окислению за счет изменения его химического состава;
- изоляция защищаемой поверхности от контакта с активными средами;
- снижение активности окружающей изделие среды;
- электрохимические.
Первые две группы способов применяются во время изготовления конструкции, а вторые – во время эксплуатации.
Методы повышения сопротивляемости
В состав сплава добавляют элементы, повышающие его коррозионную устойчивость. Такие стали называют нержавеющими. Они не требуют дополнительных покрытий и отличаются эстетичным внешним видом. В качестве добавок применяют никель, хром, медь, марганец, кобальт в определенных пропорциях.

Нержавеющая сталь AISI 304
Стойкость материалов к ржавлению повышают также, удаляя их состава ускоряющие коррозию компоненты, как, например, кислород и серу — из стальных сплавов, а железо – из магниевых и алюминиевых.
Снижение агрессивности внешней среды и электрохимическая защита
С целью подавления процессов окисления во внешнюю среду добавляют особые составы — ингибиторы. Они замедляют химические реакции в десятки и сотни раз.
Электрохимические способы сводятся к изменению электрохимического потенциала материала путем пропускания электрического тока. В результате коррозионные процессы сильно замедляются или даже вовсе прекращаются.
Пленочная защита
Защитная пленка препятствует доступу молекул активных веществ к молекулам металла и таким образом предотвращают коррозионные явления.
Пленки образуются из лакокрасочных материалов, пластмассы и смолы. Лакокрасочные покрытия недороги и удобны в нанесении. Ими покрывают изделие в несколько слоев. Под краску наносят слой грунта, улучшающего сцепление с поверхностью и позволяющего экономить более дорогую краску. Служат такие покрытия от 5 до 10 лет. В качестве грунта иногда применяют смесь фосфатов марганца и железа.
Защитные покрытия создают также из тонких слоев других металлов: цинка, хрома, никеля. Их наносят гальваническим способом.
Покрытие металлом с более высоким электрохимическим потенциалом, чем у основного материала, называется анодным. Оно продолжает защищать основной материал, отвлекая активные окислители на себя, даже в случае частичного разрушения. Покрытия с более низким потенциалом называют катодными. В случае нарушения такого покрытия оно ускоряет коррозию за счет электрохимических процессов.
Металлическое покрытие также можно наносить также методом распыления в струе плазмы.
Применяется также и совместный прокат нагретых до температуры пластичности листов основного и защищающего металла. Под давлением происходит взаимная диффузия молекул элементов в кристаллические решетки друг друга и образование биметаллического материала. Этот метод называют плакированием.
Коррозия металлов
Коррозия – разрушение поверхности сталей и сплавов под воздействием различных физико-химических факторов – наносит огромный ущерб деталям и металлоконструкциям. Ежегодно этот невидимый враг «съедает» около 13 млн. т металла. Для сравнения – металлургическая промышленность стран Евросоюза в прошлом, 2014 году произвела всего на 0,5 млн. тонн больше. И это только – прямые потери. А длительная эксплуатация стальных изделий без их эффективной защиты от коррозии вообще невозможна.
Что такое коррозия и её разновидности
Основной причиной интенсивного окисления поверхности металлов (что и является основной причиной коррозии) являются:
- Повышенная влажность окружающей среды.
- Наличие блуждающих токов.
- Неблагоприятный состав атмосферы.
Соответственно этому различают химическую, трибохимическую и электрохимическую природу коррозии. Именно они в совокупности своего влияния и разрушают основную массу металла.
Химическая коррозия
Такой вид коррозии обусловлен активным окислением поверхности металла во влажной среде. Безусловным лидером тут является сталь (исключая нержавеющую). Железо, являясь основным компонентом стали, при взаимодействии с кислородом образует три вида окислов: FeO, Fe2O3 и Fe3O4. Основная неприятность заключается в том, что определённому диапазону внешних температур соответствует свой окисел, поэтому практическая защита стали от коррозии наблюдается только при температурах выше 10000С, когда толстая плёнка высокотемпературного оксида FeO сама начинает предохранять металл от последующего образования ржавчины. Это процесс называется воронением, и активно применяется в технике для защиты поверхности стальных изделий. Но это – частный случай, и таким способом активно защищать металл от коррозии в большинстве случаев невозможно.

Химическая коррозия активизируется при повышенных температурах. Склонность металлов к химическому окислению определяется значением их кислородного потенциала – способности к участию в окислительно-восстановительных реакциях. Сталь – ещё не самый худший вариант: интенсивнее её окисляются, в частности, свинец, кобальт, никель.
Электрохимическая коррозия
Эта разновидность коррозии более коварна: разрушение металла в данном случае происходит при совокупном влиянии воды и почвы на стальную поверхность (например, подземных трубопроводов). Влажный грунт, являясь слабощёлочной средой, способствует образованию и перемещению в почве блуждающих электрических токов. Они являются следствием ионизации частиц металла в кислородсодержащей среде, и инициирует перенос катионов металла с поверхности вовне. Борьба с такой коррозией усложняется труднодоступностью диагностирования состояния грунта в месте прокладки стальной коммуникации.
Электрохимическая коррозия возникает при окислении контактных устройств линий электропередач при увеличении зазоров между элементами электрической цепи. Помимо их разрушения, в данном случае резко увеличивается энергопотребление устройств.
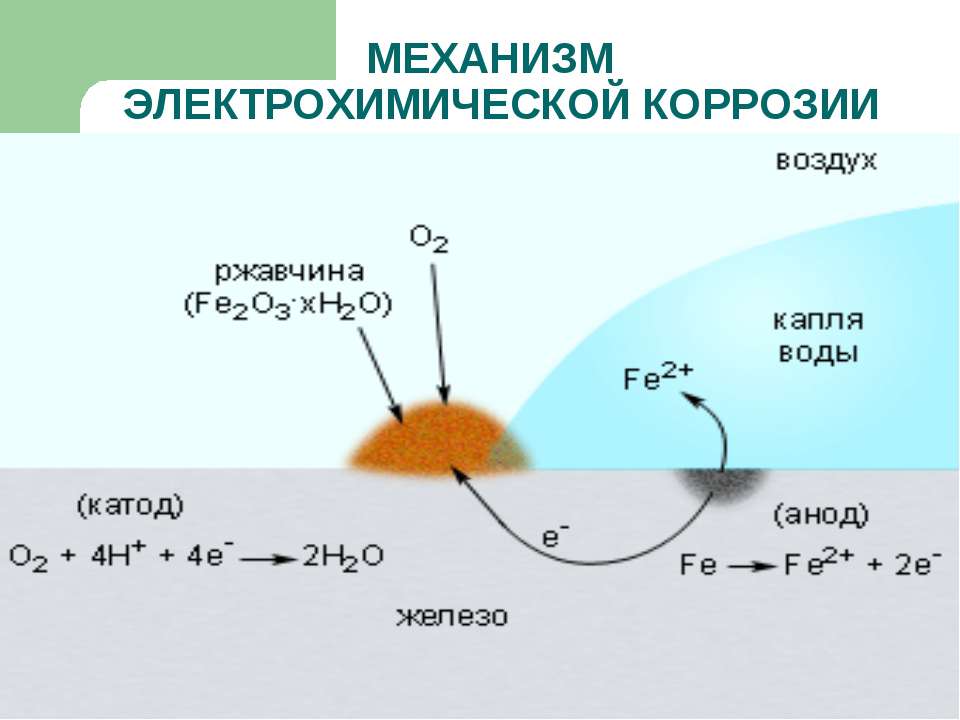
Трибохимическая коррозия
Данному виду подвержены металлообрабатывающие инструменты, которые работают в режимах повышенных температур и давлений. Антикоррозионное покрытие резцов, пуансонов, фильер и пр. невозможно, поскольку от детали требуется высокая поверхностная твёрдость. Между тем, при скоростном резании, холодном прессовании и других энергоёмких процессах обработки металлов начинают происходить механохимические реакции, интенсивность которых возрастает с увеличением температуры на контактной поверхности «инструмент-заготовка». Образующаяся при этом окись железа Fe2O3 отличается повышенной твёрдостью, и поэтому начинает интенсивно разрушать поверхность инструмента.

Методы борьбы с коррозией
Выбор подходящего способа защиты поверхности от образования ржавчины определяется условиями, в которых работает данная деталь или конструкция. Наиболее эффективны следующие методы:
- Нанесение поверхностных атмосферостойких покрытий;
- Поверхностная металлизация;
- Легирование металла элементами, обладающими большей стойкостью к участию в окислительно-восстановительных реакциях;
- Изменение химического состава окружающей среды.
Механические поверхностные покрытия
Поверхностная защита металла может быть выполнена его окрашиванием либо нанесением поверхностных плёнок, по своему составу нейтральных к воздействию кислорода. В быту, а также при обработке сравнительно больших площадей (главным образом, подземных трубопроводов) применяется окраска. Среди наиболее стойких красок – эмали и краски, содержащие алюминий. В первом случае эффект достигается перекрытием доступа кислороду к стальной поверхности, а во втором – нанесением алюминия на поверхность, который, являясь химически инертным металлом, предохраняет сталь от коррозионного разрушения.
Положительными особенностями данного способа защиты являются лёгкость его реализации и сравнительно небольшие финансовые затраты, поскольку процесс достаточно просто механизируется. Вместе с тем долговечность такого способа защиты невелика, поскольку, не обладая большой степенью сродства с основным металлом, такие покрытия через некоторое время начинают механически разрушаться.

Химические поверхностные покрытия
Коррозионная защита в данном случае происходит вследствие образования на поверхности обрабатываемого металла химической плёнки, состоящей из компонентов, стойких к воздействию кислорода, давлений, температур и влажности. Например, углеродистые стали обрабатывают фосфатированием. Процесс может выполняться как в холодном, так и в горячем состоянии, и заключается в формировании на поверхности металла слоя из фосфатных солей марганца и цинка. Аналогом фосфатированию выступает оксалатирование – процесс обработки металла солями щавелевой кислоты. Применением именно таких технологий повышают стойкость металлов от трибохимической коррозии.
Недостатком данных методов является трудоёмкость и сложность их применения, требующая наличия специального оборудования. Кроме того, конечная поверхность изменяет свой цвет, что не всегда приемлемо по эстетическим соображениям.
Легирование и металлизация
В отличие от предыдущих способов, здесь конечным результатом является образование слоя металла, химически инертного к воздействию кислорода. К числу таких металлов относятся те, которые на линии кислородной активности находятся возможно дальше от водорода. По мере возрастания эффективности этот ряд выглядит так: хром→медь→цинк→серебро→алюминий→платина. Различие в технологиях получения таких антикоррозионных слоёв состоит в способе их нанесения. При металлизации на поверхность направляется ионизированный дуговой поток мелкодисперсного напыляемого металла, а легирование реализуется в процессе выплавки металла, как следствие протекания металлургических реакций между основным металлом и вводимыми легирующими добавками.

Изменение состава окружающей среды
В некоторых случаях существенного снижения коррозии удаётся добиться изменением состава атмосферы, в которой работает защищаемая металлоконструкция. Это может быть вакуумирование (для сравнительно небольших объектов), или работа в среде инертных газов (аргон, неон, ксенон). Данный метод весьма эффективен, однако требует дополнительного оборудования — защитных камер, костюмов для обслуживающего персонала и т.д. Используется он главным образом, в научно-исследовательских лабораториях и опытных производствах, где специально поддерживается необходимый микроклимат.
Кто нам мешает, тот нам поможет
В завершение укажем и на довольно необычный способ коррозионной защиты: с помощью самих окислов железа, точнее, одного из них — закиси-окиси Fe3O4. Данное вещество образуется при температурах 250…5000С и по своим механическим свойствам представляет собой высоковязкую технологическую смазку. Присутствуя на поверхности заготовки, Fe3O4 перекрывает доступ кислороду воздуха при полугорячей деформации металлов и сплавов, и тем самым блокирует процесс зарождения трибохимической коррозии. Это явление используется при скоростной высадке труднодеформируемых металлов и сплавов. Эффективность данного способа обусловлена тем, что при каждом технологическом цикле контактные поверхности обновляются, а потому стабильность процесса регулируется автоматически.
Коррозия металла – виды и способы защиты
Коррозийные процессы представляют наиболее реальную угрозу для металлических конструкций. Вне зависимости от толщины стали, ржавчина способна быстро привести материал в негодность. В некоторых случаях, при небольших повреждениях, развитие коррозии удается остановить, а последствия ликвидировать. Чаще всего приходится менять металлические элементы полностью. Поэтому защита стали от коррозии является первоочередной задачей при строительстве и эксплуатации конструкций.
Причины и последствия образования коррозии на металле
В идеальных условиях любой металл сохраняет свои характеристики в течение длительного периода времени. Даже если в состав материала не входят дополнительные примеси, отсутствие внешних воздействий позволяет сохранять прочность и жесткость конструкции. В реальной жизни таких условий добиться практически невозможно. Коррозийные процессы могут быть вызваны следующими причинами:
- повышенная влажность воздуха, за счет которой металл постоянно подвергается значительным нагрузкам и очень быстро начинает окисляться;
- выпадение осадков на незащищенную поверхность стали также влечет за собой распространение очагов коррозии;
- часто причиной окисления металла являются блуждающие токи, присутствующие на поверхности изделия;
- атмосфера с различным содержанием химически активных элементов также может вызвать увеличение скорости распространения коррозии.

На начальном этапе окисления на поверхности металла становятся заметны яркие пятна, впоследствии металл полностью покрывается ржавчиной. Если не обращать внимания на подобные явления, со временем коррозия проникает внутрь изделия, полностью разрушая его.
Разновидности коррозийных процессов
Коррозия стали по типу может быть химической и электротехнической. В первом случае атомы металла и окислителя вступают в реакцию и образуют прочные связи. Образовавшаяся структура не проводит электричество, в отличие от первоначального состава изделия. Для электротехнической коррозии характерно полное разложение металла, который становится непригоден в дальнейшей эксплуатации.
Кроме химической и электротехнической можно выделить и другие виды коррозии:
- чаще других встречается газовая коррозия, протекающая при высокой температуре и минимальном содержании влаги в рабочей среде;
- атмосферная коррозия развивается при нахождении металлического изделия в газовой среде высокой влажности;
- биологические микроорганизмы также могут оказывать негативное влияние на прочность и целостность стальных конструкций, вызывая окисление материала;
- при взаимодействии различных металлов, состав и стационарный потенциал которых отличается, пятна ржавчины могут появиться в точках соприкосновения изделий;
- воздействие радиоактивного излучения приводит к разрушению структуры стали и развитию коррозийных процессов.

В большинстве случаев сложно выделить какой-то один вид коррозии, негативно воздействующий на состояние металлоконструкций. Разрушение и деградация стали вызвана влиянием нескольких факторов, таких как повышенная влажность, неблагоприятный состав атмосферы, биологическая активность микроорганизмов, радиационный фон. Единственным способом исключить или снизить скорость распространения коррозии является защита материала специальными составами и средствами.
Технология защиты стали от возникновения и развития коррозии
Оптимальным вариантом для исключения коррозии является использование при строительстве и монтаже специальных марок стали, неподверженных окислению. В противном случае от собственника металлоконструкций потребуется обеспечить своевременную защиту стали от окисления. Возможными вариантами подобного подхода являются:
- поверхностная обработка металла специальными составами, устойчивыми к атмосферным воздействиям;
- металлизация конструкций, также выполняемая поверхностным методом;
- легирование стали специальными составами, особенностью которых является устойчивость к окислительным процессам;
- непосредственное воздействие на окружающую химическую среду с целью изменения ее состава.

Каждая из указанных методик имеет свои достоинства и условия использования. Выбор способа зависит от текущего состояния стальной конструкции, интенсивности развития коррозии, условий эксплуатации металлических изделий.
Поверхностная обработка металла
Самым простым и наиболее распространенным способом является механическая обработка стали. Конструкция окрашивается эмалями и красками с высоким содержанием алюминия. В результате полностью перекрывается доступ окружающего воздуха к металлу. Простота и невысокая стоимость технологии являются ее основными достоинствами. К минусам можно отнести недолговечность покрытия и необходимость периодически его обновлять.
Химическая обработка металла
Отличным способом защиты стали от коррозии является ее обработка химическим способом. На поверхности создается тонкая и прочная пленка, наличие которой предотвращает проникновение к металлу влаги и других негативных сред. Технология применяется только с использованием специальных средств, а ее стоимость доступна не каждому собственнику металлоконструкций.
Металлизация и легирование
Нанесение слоя цинка, хрома, серебра или алюминия также является отличным способом обработки стали. Металлизация и легирование позволяет создать на поверхности стали дополнительный слой металла, устойчивого к воздействию окружающей среды. Способ обработки меняется в зависимости от используемого сплава, эффективность метода доказана на практике.
Изменение окружающей среды
Для многих металлоконструкций и изделий, работающих в замкнутом пространстве, гораздо выгоднее создать благоприятные условия. В таких случаях используется технология вакуумирования, в камеру закачивают различные по составу газы. В результате исключается контакт металла и окружающей среды, процессы коррозии полностью отсутствуют.
Каждая из указанных технологий имеет свой диапазон использования. При этом бороться с коррозией необходимо сразу после начала использования металлоконструкций. В противном случае окисление металла будет необратимым, изделие придется ремонтировать или полностью менять гораздо раньше требуемого срока эксплуатации.


